Imagine a seguinte situação: você está trabalhando em um projeto para registrar um novo medicamento. No início do projeto, o fabricante do IFA foi selecionado e você fez a predição de mutagenicidade para as impurezas. Todas as impurezas classe 1, 2 ou 3 estavam sendo controladas conforme ICH M7. Após o desenvolvimento e validação dos métodos analíticos, desenvolvimento da formulação, produção do piloto e estabilidade, o dossiê está finalmente pronto para a submissão. Porém já passaram mais de 2 anos desde a avaliação de mutagenicidade, e os modelos in silico foram atualizados para uma nova versão. Se você submeter a avaliação anterior, a agência reguladora pode emitir exigência solicitando que a versão mais atualizada do software seja usada.
Então antes da submissão, você roda a predição novamente, com a nova versão do software.
Qual o impacto disso?
Tem a possibilidade da classificação mudar, e uma impureza classe 5 passar a ser classe 1, 2 ou 3?
Sim, essa possibilidade existe, mas ela é muito baixa.
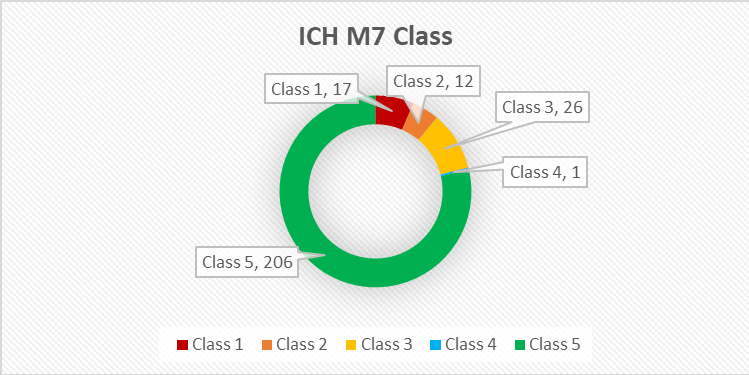
O trabalho da nossa consultora Fernanda mostrou que em um intervalo de 3 anos, para as 252 impurezas avaliadas, apenas 4 mudaram de classe, sendo que 2 eram potencialmente mutagênicas e passaram a ser não mutagênicas, e as outras duas eram classe 3 e passaram a ser classe 2 – confirmadamente mutagênicas. Em nenhum caso uma impureza classe 5 mudou para potencialmente mutagênica (Waechter et al, 2024). E o principal motivo para isso é a realização do expert review – a avaliação do especialista após cada predição in silico. Porque se o especialista tiver dúvida, ele não vai classificar como classe 5, e sim como classe 3. Assim mesmo que no futuro a base de dados seja atualizada, a chance de um novo dado mostrar que uma impureza previamente classe 5 na verdade é classe 2 é baixa.
Essa constatação foi a mesma de outros autores, como discutido por Hasselgreen et al (2020).
Quando então é necessário repetir uma predição in silico?
No trabalho por Hasselgreen et al (2020), com participação do FDA como um dos coautores, a recomendação foi de repetir a predição in silico antes da submissão regulatória apenas, não sendo necessário repetir a cada atualização do software. Porém, essa é uma decisão de cada empresa, que deve avaliar cada caso e estar ciente dos potenciais riscos.
Se você tiver qualquer dúvida sobre esse tema, ou precisa realizar uma avaliação de mutagenicidade in silico, entre em contato conosco! Você pode enviar um email para contato@integraconsultancy.com.br ou nos chamar no Whatsapp clicando em “Seja Atendido“.